

'백신 자급' 첫발...SK바이오사이언스 ‘GBP510’…세계 두번째 비교임상 방식으로 진행
임상 1상 중간분석 결과 ‘완치자 혈청 대비 5배 높은 중화항체’ 나타내
코로나바이러스감염증-19 국내 발생 현황
[전국=뉴스프리존]박나리 기자= 국내 코로나19 현황 확산세가 이어지면서 10일, 0시를 기준하여 신규 감염자 수가 다시 1천명대로 지난달 7일(1,212명)부터 35일째 네 자릿수를 이어가고 있다.
코로나바이러스감염증-19(COVID-19)관련 방역당국과 특히 수도권을 중심으로 각 지방자치단체에 따르면 18시를 기준으로 총 1,768명의 집계로 이는 전날 같은 시간에 집계된 1,170명보다 598명 많은것.
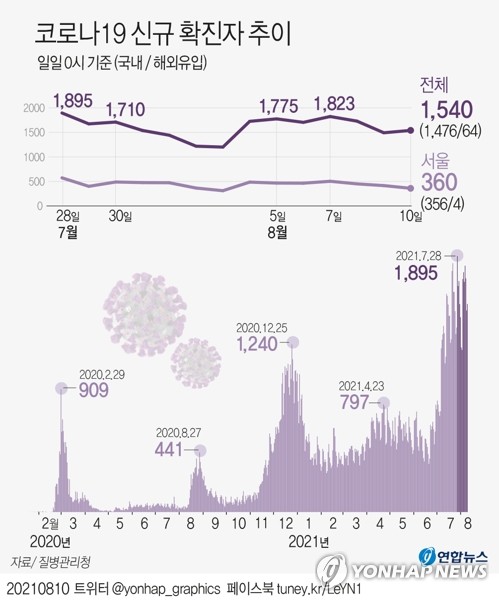
말복을 맞은 이날은 코로나19 신규감염자는 1주일 전인 지난주 화요일(8월 3일)의 18시 집계치 1,425명에 비해서는 343명 많게 나왔다.
이날 국내 발생 신규 확진자중 지역을 보면 수도권이 전체(68.5%), 서울 533명, 574명, 인천 104명으로 총 1,211명 이다.
수도권이 높게 나온 가운데, 비수도권이 전체(31.5%), 경남 110명, 부산 103명, 충남 76명, 경북 67명, 대구 55명, 충북 33명, 제주 23명, 대전 22명, 울산 18명, 광주 15명, 강원 14명, 전북·전남 각 10명, 세종 1명 총557명 이다.
코로나19 감염에 대한 집계 별로 살펴보면 신규 확진자 수는 일별로 살펴보면, (지난 7일)1,212명→1,275명→1,316명→1,378명→1,324명→1,100명→1,150명→1,615명→1,599명→1,536명→1,452명→1,454명→1,252명→1,278명→1,784명→1,842명→1,630명→1,629명→1,318명→1,365명→1,895명→1,674명→1,710명→1,539명→1,442명→1,219명→1,202명→1,725명→1,776명→1,704명→1,823명→1,729명→1,492명→1,540명을 기록해 1천400명∼1천800명대를 오르내린 가운데 최근 1주간 하루 평균 1,684명꼴로 나온 가운데 일평균 지역발생은 1천626명에 달했다.
한편, 이렇게 이날 집계를 마감하는 자정에 마감되는 만큼 새로히 시작하는 11일 0시 기준으로 발표될 신규 확진자 수는 이보다 더 늘어 2천명 안팎, 많으면 2천명대에 달할 전망이다. 전날 18시 이후 370명 늘어 최종 1,540명으로 마감됐다.
중앙방역대책본부는 수도권은 거리두기 4단계 유지로 발생이 소폭 감소 추세이나, 비수도권은 이동량이 증가(7.26∼8.1, 7.2% 증가)하고 환자가 계속 증가하고 있어 유행 억제에는 아직 불충분하다고 밝혔다.
정부는 ▲수도권 4단계, 비수도권 3단계를 유지하여 이행력을 제고, ▲감염확산 가능성이 높은 지역은 선제적 거리두기 격상, ▲환자 급증으로 방역역량 초과 지역에 대한 역학조사관, 역학조사지원 인력 파견 등 지원 강화, ▲예방접종 지속 실시 등을 추진할 계획이다. 특히 가족 내 전파는 직장, 보육 및 교육시설(어린이집·학교·학원)을 통한 추가전파로 발생 규모가 커지고, 지역사회로 확산될 가능성이 높아지고 있다. 최근 주요 집단사례를 살펴보면, ▲서울 서초구의 한 교회에서 이달 4일 첫 환자가 나온 뒤 33명이 연이어 양성 판정을 받아 누적 34명이 됐고, 경기 안산시의 한 음식점(2번째 사례)에서는 8일 이후 12명이 감염됐다. ▲충남 서산시 자동차 부품 제조업체에서는 8일 이후 종사자 14명이 확진 판정을 받았고, 전남 목포시 어선(2번째 사례)과 관련해 종사자 7명이 감염됐다. ▲학원, 주점, 실내체육시설, 목욕탕, PC방, 식당 등에서 감염 사례가 잇따랐다.
또, 백신 관련은 11일, 화이자 백신 160만 회분이 인천공항에 도착할 예정이다. 이로써 화이자 백신 413만 회분을 포함하여 이달 1일부터 11일까지 898만 회분의 백신이 도입된다. 안정적인 백신 공급을 위해 지속적으로 제약사와 긴밀히 협의해 나갈 예정이며, 구체적인 공급 일정은 제약사와 협의 되는대로 신속하게 안내할 계획이다.
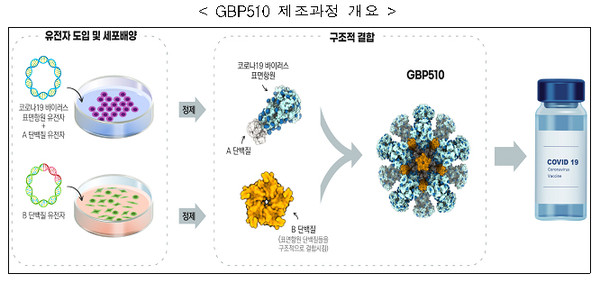
식품의약품안전처는 SK바이오사이언스가 개발하고 있는 코로나19 백신 ‘GBP510’의 3상 임상 시험계획을 승인했다고 10일 밝혔다. 국산 백신의 3상 임상시험 계획이 승인되면서 백신 자급 첫발을 내디뎠다. 임상이 잘 진행되면 내년 상반기 접종도 가능할 전망이다. 아스트라제네카(AZ) 백신과의 비교로 효과를 입증하는 비교임상 방식으로, 이는 프랑스 발네바사(社)가 개발한 코로나19 백신의 아스트라제네카 백신에 대한 비교 임상에 이어 세계에서 두 번째다. GBP510은 유전자 재조합 기술을 이용해 만든 코로나19 바이러스의 표면항원 단백질을 주입해 면역반응을 유도하는 ‘재조합 백신’이다. 표면항원 단백질을 투여하면 체내에서 면역세포를 자극해 중화항체 생성을 유도하며, 인체에 코로나19 바이러스가 침입했을 때 바이러스를 중화해 제거하게 된다. 중화항체는 특정 바이러스를 중화할 수 있는 항체를 말한다. 이 백신은 특히 항원 노출을 증가시키는 기술을 활용해 항체를 많이 생성함으로써 면역효과를 높일 수 있도록 개발됐다고 식약처는 설명했다. 이번에 승인한 3상 임상시험은 18세 이상의 성인을 대상으로 GBP510의 면역원성과 안전성을 평가하기 위한 임상시험이다. 3상 임상시험은 국내에서 허가돼 예방접종에 사용하고 있는 ‘아스트라제네카코비드-19백신주’를 대조백신으로 사용해 시험 백신의 효과를 확인하는 비교임상 방식으로 진행된다. |
|---|










 홈
사회
홈
사회
